↓bottom↓
James JOULE (UK, 1818-1889)
«Vi sorprenderà quindi sapere che, fino a pochissimo tempo fa, era opinione universale che la forza viva (quella che in termini moderni chiamiamo energia) potesse essere assolutamente e irrevocabilmente distrutta ad arbitrio di chiunque. Quando un peso cade a terra, dunque si supponeva che la sua forza viva venisse totalmente annichilita, e che il lavoro eventualmente speso per portarlo alla quota da cui è caduto fosse interamente gettato via e sprecato, senza produrre il benché minimo effetto.» James Joule, 1847
...
 principio di conservazione dell'energia - 1847
principio di conservazione dell'energia - 1847
Joule, osservò quello che accadeva nei vecchi mulini ad acqua:
il liquido scorreva velocemente sulla sommità di una ruota a pale ed emergeva al fondo ad una velocità inferiore.
Parte della sua "vis viva" era stata spesa per far girare la ruota
così anche negli esperimenti con i cannoni di Rumford il moto circolare dei trapani veniva convertito in un diverso tipo di moto: minuscole vibrazioni materiali che percepiscono come calore
insomma l'energia non era mai distrutta, ma solo trasformata in una diversa forma di energia, compreso il calore ormai interpretabile come una forma di energia (principio di conservazione dell'energia - 1847)
il passo ulteriore sarebbe quello di misurare quanto lavoro occorre per produrre una data quantità di calore...
richiamo:
 la CONSERVAZIONE dell'energia meccanica con lo skateboard (simulazione PhET)
la CONSERVAZIONE dell'energia meccanica con lo skateboard (simulazione PhET)
l'EQUIVALENTE MECCANICO DELLA CALORIA
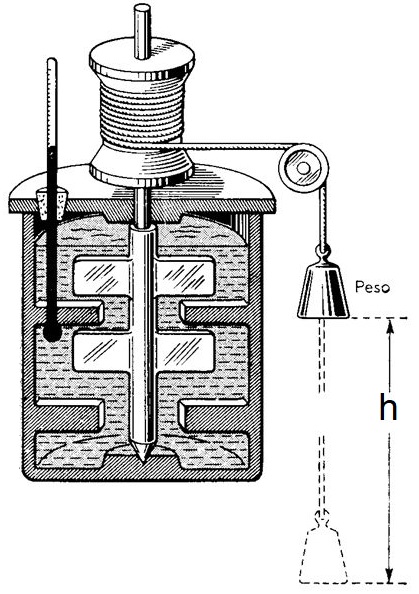
dopo vari tentativi Joule costruì un dispositivo detto il "mulinello di Joule" (1847) che permette di misurare quanta energia meccanica è necessaria per aumentare la temperatura dell'acqua ossia: "l'EQUIVALENTE MECCANICO DELLA CALORIA":
l'idea dell'esperimento è semplice:
dissipare una quantità nota di energia meccanica (facendo cadere una massa nota)
all'interno di una massa d'acqua termicamente isolata (mediante della pale ruotanti)
e misurare l'aumento di temperatura
quindi se si riescono ad eliminare, o ridurre al minimo, attriti e dissipazioni di energia, per il principio di conservazione dell'energia, si ha:
calore acquisito dall'acqua = energia meccanica dissipata nella caduta del peso
nel 1825 era stata definita la caloria come la quantità di calore necessaria per innalzare la temperatura di 1 grammo di acqua distillata da 14,5°C a 15,5°C alla pressione atmosferica (cal non è una unità di misura S.I., ma è ancora utilizzata)
con il suo mulinello Joule misurò che:
1 Cal = 4186 J
[detto EQUIVALENTE MECCANICO della CALORIA]
(occorre tenere presente che Joule misurava gli esiti dei suoi esperimenti in piedi, °F, once e per il lavoro in piedi-libbre e che i primi valori trovati furono poi migliorati negli anni)
- - -
Quindi il calore può essere considerato una forma di energia o meglio un modo per trasferire energia e si può misurare con le stesse unità di misura dell'energia
inoltre vale il principio di conservazione dell'energia
un esperimento per misurare l'equivalente meccanico della caloria:
in termini moderni (e per gli esercizi) si può utilizzare La legge fondamentale della TERMOLOGIA
ovvero il legame tra TEMPERATURA T [K] e CALORE E [J]
ΔE = c·m· ΔT
in cui m è la massa [kg]
e c è il calore specifico del corpo [J/(K·kg)]
definito come la quantità di energia che si deve fornire ad 1kg di materia per aumentarne la temperatura di 1K
 TABELLA di calori specifici (link)
TABELLA di calori specifici (link)
il calore specifico dell'acqua è: c = 4186 J / (kg·K)
un valore molto alto... insomma scaldare l'acqua è costoso quanto spostarla...
- - -
Riducendo ogni dispersione (per il principio di conservazione dell'energia) si potrebbe trasformare in calore tutta l'energia meccanica:
Q = U
c·macqua·ΔT = mlasciata cadere·g·h
quindi ΔT =....... prova TU.....
 un esercizio sul mulinello di Joule (link)
un esercizio sul mulinello di Joule (link)
- - -
 l'esperimento di Joule in video:
l'esperimento di Joule in video:
- - -
Esercizi sul mulinello di Joule (Vol.2 pag.459)
Per quanto detto, secondo Joule, l'acqua ai piedi di una cascata dovrebbe essere leggermente più calda di quella in cima in quanto l'energia potenziale dell'acqua si dovrebbe trasformare in calore ai piedi della cascata, secondo i calcoli la cascata Arpenaz in Francia, alta 365 metri, dovrebbe esibire una differenza di temperatura di quasi mezzo grado, ma tale differenza non era misurabile non solo a causa degli spruzzi, ma anche perchè una cascata non è un sistema termicamente isolato inoltre andrebbe computata anche la differenza di energia cinetica tra l'acqua in alto ed in basso, insomma praticamente impossibile da calcolare, ma in linea teorica Joule ha ragione: l'acqua ai piedi di una cascata è leggermente più calda di quella in cima... di quanto?
Q = U
c·macqua caduta ·ΔT = macqua caduta·g·h
quindi ΔT =....... prova TU.....
 un esercizio sulla cascata di Joule (link)
un esercizio sulla cascata di Joule (link)
CONCLUSIONI
Energia, lavoro e calore dunque, non solo erano parenti, ma erano aspetti differenti dello stesso fenomeno e....
- hanno la stessa unità di misura [J]
- sono modi diversi in cui la "vis viva", l'energia, viene convertita in movimento.
Si trattava di una idea straordinaria: quando si solleva un peso da terra si spende energia che viene restituita quando questo cade. Similmente, collegando un generatore, il lavoro meccanico può essere convertito in energia elettrica sfruttabile per alimentare un motore e pompare acqua in un serbatoio sopraelevato e poi cadendo l'acqua poteva azionare un mulino che a sua volta poteva essere usato per azionare una macina. Ma ad ogni passaggio, una frazione di energia sarebbe andata inevitabilmente dispersa in calore; e se un peso veniva semplicemente lasciato cadere senza fargli compiere lavoro, si sarebbe ottenuto solo calore a causa dell'impatto con il terreno e dell'attrito con l'aria...
dunque non era il calorico l'entità che si conservava, ma l'ENERGIA.
Una volta accettata la scoperta di Joule, William Thomson (lord Kelvin) si mise a studiare le implicazioni. Il calore non sparisce dall'universo, ma diventa inutilizzabile poiché passa dal caldo al freddo e non torna mai più indietro... è irrevocabilemten perduto. Questo significava che il mondo era stato un tempo estremamente caldo e sarebbe diventato inevitabilmente più freddo; "un certo numero di secoli fa la Terra deve essere stata - e tra un certo numero di secoli sarà di nuovo - inadatta alla vita"
Lo stesso dovava valere per l'universo intero: ha avuto un inizio e da allora il suo percorso è stato in discesa... e tutto ciò per aver tentato di capire come funzionano le macchine a vapore...
↑top↑